เราทำความเข้าใจเกี่ยวกับการเร่งปฏิกิริยาทั้งปฏิกิริยาเอกพันธุ์และวิวิธพันธุ์ซึ่งเป็นปฏิกิริยาที่ใช้ในการเตรียมสารผลิตภัณฑ์ในโรงงานอุตสาหกรรมหรือเป็นปฏิกิริยาที่เกิดภายนอกร่างกายของสิ่งมีชีวิตไปแล้ว ถึงตอนนี้เราจะมาทำความเข้าใจการเร่งปฏิกิริยาที่เกิดขึ้นภายในร่างกายของสิ่งมีชีวิตกันบ้าง
แน่นอนว่า ปฏิกิริยาต่างๆ เหล่านั้นอาจจะเกิดด้วยอัตราที่ช้ากว่าปกติ 106 ถึง 1012 เท่า เราจะได้สารอาหารหรือพลังงานเพียงพอที่จะใช้ในการดำรงชีวิตหรือไม่ เอนไซม์ (enzyme) คือ ตัวเร่งปฏิกิริยาชีวภาพ (biological catalyst) ที่ช่วยเร่งปฏิกิริยาทางชีวภาพให้มีอัตราการเกิดปฏิกิริยาสูงขึ้นประมาณ 106 ถึง 1012 เท่า และเอนไซม์ยังมีความจำเพาะเจาะจงต่อปฏิกิริยาสูงมาก คือ เอนไซม์จะเลือกทำปฏิกิริยากับโมเลกุลของสารตั้งต้นหรือสับสเตรท (substrate) บางชนิดเท่านั้น บางทีเราอาจจะจัดว่า การเร่งปฏิกิริยาด้วยเอนไซม์เป็นการเร่งปฏิกิริยาวิวิธพันธุ์ เพราะเอนไซม์ที่ใช้ในอุตสาหกรรมจะถูกตรึง (immobilized) อยู่บนของแข็ง เช่น ซิลิกาเจล และเอนไซม์ในสิ่งมีชีวิตจะเกาะอยู่กับโครงสร้างที่เป็นของแข็งในเซลล์
แบบจำลองแม่กุญแจ-ลูกกุญแจ (lock-and-key theory) เอนไซม์จะมีบริเวณเร่ง (active site) ที่มีโครงสร้างเหมาะสมกับโครงสร้างโมเลกุลของสับสเตรท เหมือนกับลูกกุญแจที่มีโครงสร้างเหมาะสมกับแม่กุญแจ จึงจะไขแม่กุญแจได้พอดี ซึ่งเราเรียกทฤษฎีนี้ว่า ทฤษฎีแม่กุญแจ-ลูกกุญแจ (lock-and-key)
แต่แบบจำลองนี้ขัดแย้งกับการศึกษาต่อมาซึ่งแสดงให้เห็นว่า เอนไซม์แต่ละชนิดอาจยึดกับสับสเตรทที่มีรูปร่างใกล้เคียงกันได้ เพราะเอนไซม์เป็นโปรตีนและมีความยืดหยุ่น ไม่ได้มีโครงสร้างแข็งเหมือนลูกกุญแจ เอนไซม์จึงสามารถปรับรูปร่างให้จับกับสับสเตรทได้ดี
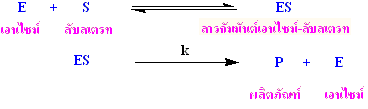
เราสามารถเขียนสมการแสดงกลไกอย่างง่ายในการทำงานของเอนไซม์ได้ดังนี้
เมื่อ
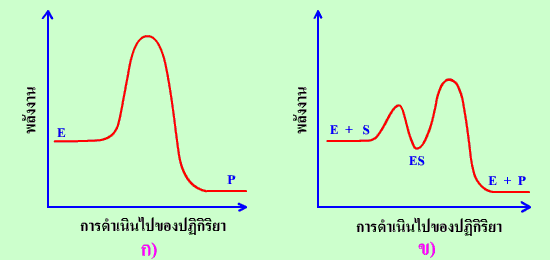
E คือ เอนไซม์ (enzyme) ในการเกิด ES และการสลายตัวของ ES กลับไปเป็นโมเลกุลของเอนไซม์และสับสเตรทนั้นเกิดขึ้นได้เร็วมาก ส่วนการเกิดสารผลิตภัณฑ์ในขั้นที่สองนั้นจะเกิดได้ช้ากว่าจึงเป็นขั้นกำหนดอัตรา
การเปรียบเทียบระหว่าง
โดยทั่วไปแล้ว เราสามารถหาอัตราการเกิดปฏิกิริยาที่เร่งโดยเอนไซม์แบบนี้ได้จากสมการ
ความเข้มข้นของ ES จะขึ้นอยู่กับปริมาณของสับสเตรท ดังแสดงในกราฟ 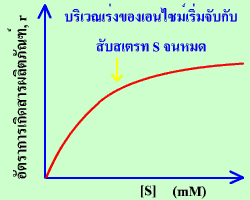 ความสัมพันธ์ระหว่างอัตราการเกิดสารผลิตภัณฑ์กับความเข้มข้นของสับสเตรทในปฏิกิริยาที่มีเอนไซม์เป็นตัวเร่งปฏิกิริยา จากกราฟ ในช่วงแรกอัตราจะเพิ่มขึ้นตามความเข้มข้นของสับสเตรทอย่างรวดเร็ว แต่เมื่อความเข้มข้นเพิ่มขึ้นถึงค่าหนึ่ง บริเวณเร่งของเอนไซม์ถูกใช้หมด ปฏิกิริยาก็จะกลายเป็นอันดับศูนย์เมื่อเทียบกับสับสเตรท นั่นก็หมายความว่าอัตราการเกิดปฏิกิริยาจะคงที่ไม่ว่าความเข้มข้นของสับสเตรทจะเพิ่มขึ้นสูงเพียงใด ดังนั้น เมื่อผ่านจุดนี้ไปแล้ว อัตราการเกิดผลิตภัณฑ์จะขึ้นอยู่กับความเร็วในการแตกตัวของ ES เท่านั้น ไม่ขึ้นกับจำนวนโมเลกุลของสับสเตรทที่มีอยู่ |