| |
2. พลังงานของการเปลี่ยนวัฏภาค
เราทราบกันดีแล้วว่า
สสาร มี 3 สถานะ คือ ของแข็ง ของเหลว และแก๊ส แต่ในธรรมชาติแล้ว ซึ่งมีความดันและอุณหภูมิเกือบจะคงที่
หรืออาจจะกล่าวได้ว่า ในช่วงเวลาสั้นๆ การเปลี่ยนแปลงของความดันและอุณหภูมิในบรรยากาศมีค่าน้อยมากๆ
เราจะพบว่า สารแต่ละชนิดจะปรากฏรูปให้เห็นเพียงสถานะเดียว ซึ่งอาจจะอยู่ในสถานะใดสถานะหนึ่งใน
3 สถานะที่ได้กล่าวมา เช่น น้ำที่ความดันบรรยากาศจะเป็นของเหลว คาร์บอนไดออกไซด์จะเป็นแก๊ส
เป็นต้น พบว่า เมื่อมีการเปลี่ยนแปลงของอุณหภูมิและความดันที่มีต่อสสาร สิ่งที่เกิดขึ้นก็คือ
จะทำให้สถานะของสสารเปลี่ยนจากสถานะหนึ่งไปสู่อีกสถานะหนึ่งได้
กราฟการให้ความร้อน (heating curve)
เพื่อต้องการสังเกตการเปลี่ยนแปลงสถานะของสาร
ในทางปฏิบัติ สถานะของสารตั้งต้นจะเป็นของแข็ง และมักจะทำการเพิ่มอุณหภูมิภายใต้สภาวะความดันคงที่
พิจารณากราฟการเพิ่มความร้อนต่อไปนี้
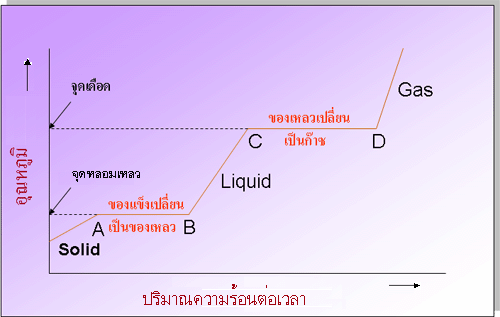
จากกราฟ
เมื่อเราเพิ่มอุณหภูมิให้แก่สารซึ่งมีสถานะเป็นของแข็ง สิ่งที่เกิดขึ้น คือ
ของแข็งจะเริ่มหลอมเหลว และสถานะของสารจะเริ่มมีการเปลี่ยนแปลงจากของแข็งไปสู่สถานะที่เป็นของเหลว
จนถึงจุดที่อุณหภูมิมีค่าคงที่ ซึ่งเป็นการเปลี่ยนแปลงจากจุด A ไป จุด B
เรียกว่า การหลอมเหลว (melting) ปริมาณความร้อนที่ใช้ในการเปลี่ยนสถานะจากของแข็งไปเป็นของเหลว
เรียกว่า ความร้อนแฝงของการหลอมเหลว และเรียกอุณหภูมิ ณ จุดนี้ว่า จุดหลอมเหลวของสาร
เมื่อสารกลายเป็นของเหลวหมดแล้ว อุณหภูมิของของเหลวจะเพิ่มขึ้นอีกเรื่อยๆ
ของเหลวเริ่มมีการเปลี่ยนแปลงสถานะจากของเหลวไปเป็นแก๊ส ซึ่งอุณหภูมิก็จะมีค่าคงที่
ซึ่งเป็นการเปลี่ยนแปลงจากจุด C ไปจุด D กระบวนการที่เกิดขี้น เรียกว่า การกลายเป็นไอ
(vaporization process) การที่สารยังมีการดูดพลังงานเข้าไปนั้น ก็เพื่อจะไปสลายแรงยึดเหนี่ยวของของเหลว
เพื่อให้กลายเป็นแก๊ส เราเรียกความร้อนนี้ว่า ความร้อนแฝงของการกลายเป็นไอ
และเรียกอุณหภูมิ ณ จุดนี้ว่า จุดเดือด
คำถามชวนให้คิด
1. การที่กล่าวมาข้างต้น สารสามารถเปลี่ยนสถานะจากสถานะหนึ่งไปสู่อีกสถานะหนึ่งได้โดยการเปลี่ยนแปลงอุณหภูมิและความดัน โดยทั่วไป เรานิยมเปลี่ยนที่อุณหภูมิมากกว่าที่จะมีการเปลี่ยนความดัน นักเรียนทราบหรือไม่ว่า เพราะเหตุใดจึงไม่นิยมที่จะเปลี่ยนความดัน?
2. จากกราฟการให้ความร้อน (heating curve) ปริมาณความร้อนต่อหนึ่งหน่วยเวลาที่ให้แก่สารจะต้องมีค่าคงที่ตลอดเวลาการทดลอง ถามว่า ถ้าเราให้ปริมาณความร้อนต่อหนึ่งหน่วยเวลามาก หรือ น้อยกว่า อยากทราบว่า ช่วง AB และ CD จะเป็นอย่างไร?
จากคำถามทั้งสองข้อที่ให้ไป นักเรียนลองเอาไปคิด และไตร่ตรอง หาคำตอบเอง
Molar
heat of fusion (![]() )
มีหน่วยเป็น kJ หมายถึง ความร้อนที่ใช้ในการหลอมเหลวสาร 1 โมล สารแต่ละชนิด
จะมีค่า molar heat of fusion ไม่เท่ากัน ซึ่งแสดงดังตาราง ต่อไปนี้
)
มีหน่วยเป็น kJ หมายถึง ความร้อนที่ใช้ในการหลอมเหลวสาร 1 โมล สารแต่ละชนิด
จะมีค่า molar heat of fusion ไม่เท่ากัน ซึ่งแสดงดังตาราง ต่อไปนี้
ชนิดของสาร |
จุดเดือด
(oC)* |
|
| อาร์กอน (Ar) | -190 |
1.3 |
| เบนซีน (C6H6) | 5.5 |
10.9 |
| เอทานอล (CH3CH2OH) | -117.3 |
7.61 |
| ไดเอทิลอีเทอร์ (C2H5OC2H5) | -116.2 |
6.90 |
| ปรอท (Hg) | -39 |
23.4 |
| มีเทน (CH4) | -183 |
0.84 |
| น้ำ (H2O) | 0 |
6.01 |
* เป็นค่าแสดงที่ความดัน 1 บรรยากาศ