ในที่นี้จะกล่าวถึงผลกระทบของก๊าซมลพิษบางตัวที่มีต่อสิ่งแวดล้อมและสุขภาพมนุษย์
คาร์บอนมอนอกไซด์ (CO) เป็นก๊าซที่เกิดขึ้นจากการเผาไหม้ไม่สมบูรณ์ของสารประกอบคาร์บอน
เป็นก๊าซที่ไม่มีสีรสและกลิ่นเบากว่าอากาศทั่วไป เมื่อหายใจเข้าไป ก๊าซนี้จะรวมตัวฮีโมโกลบิน
(haemoglobin) ในเม็ดเลือดแดงได้มากกว่าออกซิเจนถึง 200-250 เท่า เกิดเป็นคาร์บอกซีฮีโมโกลบิน
(Carboxyhemoglobin) ทำให้เม็ดเลือดแดงไม่สามารถรับ O2ได้ตามปกติร่างกายได้รับ O2 น้อยลงและหัวใจ
ต้องสูบฉีดโลหิตมากขึ้น เพื่อทำให้โลหิตผ่านปอดมากขึ้น จะได้มีการรับ O2ให้มากขึ้นหัวใจและปอดจะต้อง
ทำงานหนักขึ้น อาการทั่วไปเมื่อร่างกายได้รับ CO คือ วิงเวียนศีรษะหายใจอึดอัด คลื่นไส้อาเจียน ปวดศีรษะ
มึนงง หากร่างกายได้รับคาร์บอนไดออกไซด์มากอาจช็อกหมดสติหรือตายได้
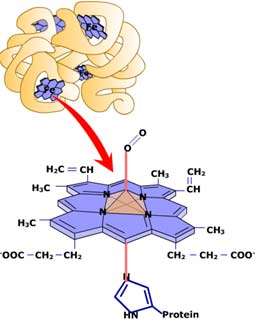
รูปที่ 2.6 ภาพของฮีโมโกลบิน
แสดงให้เห็นส่วนฮีมซึ่งจะจับ O2ตามปกติ เมื่อมี COในอากาศ CO จะไปแย่ง O2จับกับฮีโมโกลบิน
ทำให้ร่างกายขาด O2
ก๊าซออกไซด์ของไนโตรเจน ออกไซด์ของไนโตรเจนประกอบด้วยไนตรัสออกไซด์ (NOS)
ไนตริกออกไซด์ (NO) ไดไนโตรเจนไตรออกไซด์ (N2O3) ไนโตรเจนไดออกไซด์ (N2O) ไดไนโตรเจน
เตตรอกไซด์ (N2O4) และไดไนโตรเจนเพนตอกไซด์
(N2O5)
โดยทั่วไปก๊าซที่ทำให้เกิดมลพิษ
ทางอากาศ คือ ก๊าซไนตริกออกไซด์ (NO) และก๊าซไนโตรเจนไดออกไซด์ ( NO2)
ก๊าซไนตริกออกไซด์ (NO) เป็นก๊าซเฉื่อยมีคุณสมบัติเป็นยาสลบ เป็นก๊าซ
ไม่มีสีและไม่มีกลิ่น ในธรรมชาติทั่วไปพบในปริมาณน้อยกว่า 0.5 ppm. ละลายน้ำได้เล็กน้อย ส่วนไนโตรเจน
ไดออกไซด์ ( NO2) เป็นก๊าซสีน้ำตาล ถ้ามีจำนวนมากจะมองเห็น ก๊าซทั้งสองชนิดจะเกิดขึ้นเองตามธรรมชาติ
ิได้แก่ ฟ้าผ่า ฟ้าแลบ ภูเขาไฟระเบิด หรืออาจเกิดจากกลไกของจุลินทรีย์ และนอกจากนี้อาจเกิดจากมนุษย์
เช่น จากอุตสาหกรรม เช่น อุตสาหกรรมผลิตกรดไนตริก และกรดกำมะถัน และโรงงานผลิตวัตถุระเบิด และ
การเผาไหม้เของเครื่องยนต์ เป็นต้น
ก๊าซไนตริกออกไซด์ทำปฏิกิริยากับโอโซนในบรรยากาศจะเกิดเป็นไนโตเจนไดออกไซด์และออกซิเจน
ในทางตรงกันข้าม เมื่อมีแสงแดดจะทำให้ไนโตรเจนออกไซด์เกิดปฏิกิริยาผันกลับ
NO + O 3  NO 2+ O 2 NO 2+ O 2 |
โดยทั่วไป ก๊าซ NO2 ไม่เป็นอันตรายต่อร่างกาย เกิดอันตราย แต่ NO2 จะรวมตัวกับน้ำในอากาศเป็น HNO3
(กรดไนตริก) ซึ่งมีฤทธิ์กัดกร่อน
ซัลเฟอร์ออกไซด์ (SOx) ออกไซด์ซัลเฟอร์ประกอบด้วย SO2 และ SO3 โดยทั่วไปมักเขียนแทน
ซัลเฟอร์ออกไซด์
ด้วย SOx
ซัลเฟอร์ไดออกไซด์ (SO2) เป็นก๊าซไม่มีสี ไม่ติดไฟ มีกลิ่นแสบจมูก ละลายได้ดีในน้ำโดยจะเปลี่ยนเป็น
กรดซัลฟูริก ในธรรมชาติทั่วไปจะมีปริมาณน้อยในบรรยากาศคือ 0.02 - 0.1 ppm. แต่ถ้าพบในปริมาณสูงแล้ว
ส่วนมากจะเกิดจากการเผาไหม้ โดยใช้เชื้อเพลิงหรือวัสดุที่มีกำมะถันเป็นส่วนประกอบปฏิกิริยาการเกิดซัลเฟอร์
ไดออกไซด์ (SO2)
S + O2  SO2
SO2 |
ถ้า SO2ทำปฏิกริยากับ O2ในอากาศจะได้ SO3 ยิ่งถ้าในบรรยากาศมีตัวเร่งปฏิกิริยาเช่น มังกานีส เหล็ก
หรือกลุ่ม
metallic oxide จะทำ ให้ปฏิกริยาเร็วขึ้น
| ตัวเร่ง |
SO2+
1/2O2  SO3
SO3 |
ถ้าในบรรยากาศ มีละอองน้ำหรือความชื้นสูง SO2จะเกิดการรวมตัวเป็นฝนกรด (acid rain) ซึ่งจะส่งผลกระทบ
ต่อระบบนิเวศ ป่าไม้ แหล่งน้ำ สิ่งมีชีวิตและมีฤทธิ์กัดกร่อนอาคาร
| |
2SO2
+ 2H 2O + O2  H
2 SO4
SO3 H
2 SO4
SO3 + H 2O  H
2SO4 H
2SO4 |
Smog (ควัน)
ควันมีทั้งควันดำและควันขาว
ควันดำ คือ อนุภาคของคาร์บอนเป็นผงหรือ เขม่าเล็ก ๆ ที่เหลือจากการเผาไหม้ของ
เครื่องยนต์ที่มีการใช้น้ำมันดีเซลเป็นส่วนใหญ่ และจากโรงงานอุตสาหกรรม
ควันขาวคือสารไฮโดรคาร์บอนหรือน้ำมันเชื้อเพลิงที่ยังเผาไหม้ไม่สมบูรณ์ ซึ่งจะปล่อยออกมาทาง
ท่อไอเสีย สารไฮโดรคาร์บอนเหล่านี้อาจเกิดปฏิกิริยาต่อจนได้เป็นก๊าซโอโซนในบรรยากาศเมื่อได้รับแสงอาทิตย์
เป็นตัวเร่งปฏิกิริยา
ฝนกรด
ฝนกรด
หมายถึง น้ำฝนที่มีค่า pH ต่ำกว่า 5.6 โดยส่วนมากเกิดจากก๊าซ 2 ชนิด คือ
1. ก๊าซซัลเฟอร์ไดออกไซด์ (SO2) ทำให้เกิดกรด ซัลฟุริก (H2SO4)
2. ออกไซด์ของไนโตรเจน (NOx) ทำให้เกิดกรด ไนตริก (HNO3)
ฝนกรดมักพบในเขตอุตสาหกรรมซึ่งสามารถอยู่ในรูปของฝน หมอก หิมะ ซึ่งมีผลกระทบต่อพืช
สัตว์น้ำ
และ
สิ่งก่อสร้างต่างๆ
กลไกการเปลี่ยนจากก๊าซ SO2 และ NOx เป็นกรด เกิดได้ทั้งในสถานะก๊าซและของเหลว
1.ก๊าซซัลเฟอร์ไดออกไซด์ (SO2) ปฎิกิริยาของซัลเฟอร์ไดออกไซด์กับออกซิเจนในบรรยากาศ ดังนี้
| |
S (ในถ่านหิน)+O2  SO2 SO2
SO2 + O2  2SO3 2SO3
SO3+H2O  H2SO4 H2SO4 |
2. ออกไซด์ของไนโตรเจน (NOx)
โดยปกติทั้ง O2 และ NO2 เป็นก๊าซที่ไม่ว่องไวในการเกิดปฏิกิริยาแต่ถ้าอยู่ภายใต้อุณหภูมิและ
ความดันสูงก๊าซทั้งสองชนิดจะทำปฏิกิริยากันเกิดเป็น nitrogen dioxide ( NO2)
N2(gas) + O2 (gas) + พลังงาน  2 NO (gas) 2 NO (gas) |
จากนั้น NO จะทำปฏิกิริยากับ O2 ในบรรยากาศได้ nitrogen dioxide (NO2)
2 NO (gas) + O2 (gas)  2 NO2 (gas) 2 NO2 (gas) |
NO2เป็นก๊าซพิษมีน้ำตาล และเป็นก๊าซที่ว่องไวในการทำปฏิกิริยา ซึ่งจะทำปฏิกิริยากับอนุมูลอิสระ
ของหมู่ hydroxyl (OH) ในบรรยากาศได้กรดไนตริก HNO3 ซึ่งจะละลายในน้ำ
NO2(gas) + OH (gas)  HNO3 (gas) HNO3 (gas) |
ผลกระทบของฝนกรด ฝนกรดมีผลกระทบต่อพืชและทรัพยากรธรรมชาติ กล่าวคือ ฝนกรดสามารถทำปฎิกิริยากับธาตุอาหาร
ที่สำคัญของพืช เช่น แคลเซียม, ไนเตรต, แมกเนเซียม และ โปรแตสเซียม ทำให้พืชไม่สามารถนำธาตุอาหาร
เหล่านี้ไปใช้ได้
และซัลเฟอร์ไดออกไซด์ในบรรยากาศยังไปปิดปากใบพืช ซึ่งจะมีผลกระทบต่อการหายใจของพืช
ความเป็นกรดที่เพิ่มขึ้นของน้ำยังมีผลกระทบด้านระบบนิเวศ ที่อยู่อาศัยรวมถึงการดำรงชีวิตอีกด้วย
ฝนกรดสามารถละลาย calcium carbonate ในหินทำให้เกิดการสึกกร่อน เช่น ปิรามิดในประเทศอียิปต์
์ และ ทัชมาฮาลในประเทศอินเดีย เป็นต้น นอกจากนี้ยังมีฤทธิ์กัดกร่อนทำลายพวกโลหะทำให้เกิดสนิมเร็วขึ้น
อีกด้วย
รูปที่ 2.7 การเกิดฝนกรดและผลกระทบที่มีต่อสิ่งแวดล้อม เช่น การกัดกร่อนของหิน
การสลายตัวของ
หินปูน และโครงสร้างของอาคาร รวมทั้งผลต่อระบบหายใจของมนุษย์
ผลกระทบจากฝนกรด อาจสรุปได้ดังนี้คือ
1. ฝนกรดจะทำลายธาตุอาหารบางชนิดในดิน เช่น ไนเตรต ฟอสเฟต ทำให้ดินเป็นกรดเพิ่มขึ้น
มีผลต่อการ เพาะปลูก เช่นผลผลิตของพิชน้อยกว่าปกติ เพราะฝนกรดทำให้ดินเปรี้ยวจุลินทรีย์หลายชนิดในดิน
ที่มีประโยชน์ต่อ การเจริญเติบโตของพืชถูกทำลาย ซึ่งจะมีผลกระทบในแง่การย่อยสลายในดินและการเจริญ
เติบโตของพืช
2. ฝนกรดทำลายวัสดุสิ่งก่อสร้างและอุปกรณ์บางชนิด คือ จะกัด กร่อนทำลายพวกโลหะ เช่น
เหล็กเป็นสนิม เร็วขึ้น สังกะสีมุงหลังคา ที่ใกล้ ๆ โรงงานจะ ผุกร่อนเร็ว สังเกตได้ง่าย นอกจากนี้ยังทำให้
แอร์
ตู้เย็น หรือวัสดุอื่น ๆ เช่นปูนซีเมนต์หมดอายุเร็วขึ้น ผุกร่อนเร็วขึ้น เป็นต้น
3. ฝนกรดจะทำลายทรัพยากรธรรมชาติ เช่น ปู หอย กุ้ง อาจมีจำนวนลดลงหรือสูญพันธุ์ไปได้
เพราะ ฝนกรดที่เกิดจากก๊าซซัลเฟอร์ไดออกไซด์และเกิด จากก๊าซไนโตรเจนอ๊อกไซด์ จะทำให้น้ำในแม่น้ำ
ทะเลสาบ มีความเป็นกรดเพิ่มขึ้น ถ้าเกิดอย่างรุนแรงอาจทำให้สัตว์น้ำดังกล่าวตาย เช่น อเมริกาตอนกลาง
ค่า PH ของน้ำในทะเลสาบลดลง ทำให้ทะเลสาบ 85 แห่ง ไม่มีปลาซึ่งเหตุการณ์ทำนองนี้เกิดขึ้นใน
ทะเลสาบ ในประเทศ สวีเดน ทะเลสาบบางแห่ง ป้องกัน ตัวเองจาก ฝนกรดได้เพราะในทะเลสาบนั้นมีสารพวก
ไบคาร์บอเนต
หรือแร่ธาตุอื่นละลายอยู่
การควบคุมและป้องกัน
ลดการใช้เชื้อเพลิงฟอสซิลให้น้อยลง จะสามารถทำให้ค่าความเป็นกรดในน้ำฝนลดลงได้
ในช่วงที่ฝนตกใหม่ๆ น้ำฝนจะไม่สะอาดมีความเป็นกรดสูง คือ pH อยู่ระหว่าง 3.5-5.0
VOCs ( volatile organic compound)
1. สารอินทรีย์ไอระเหย (Volatile Organic Chemicals, VOCs) คือ กลุ่มสารประกอบอินทรีย์
ที่ระเหย
เป็นไอได้ง่าย ที่อุณหภูมิและความดันปกติ โมเลกุลประกอบด้วยอะตอมของคาร์บอนและไฮโดรเจน
เป็นสำคัญ
ซึ่งอาจมีอะตอม ของออกซิเจนหรือ คลอรีนร่วมด้วย VOCs เป็นองค์ประกอบในผลิตภัณฑ์
หลายอย่าง
ในชีวิต
ประจำวัน เช่น สีทาบ้าน ควันบุหรี่ สารฟอกสี สารตัวทำละลายในหมึกพิมพ์ สีรถยนต์
สารโรงงานอุตสาหกรรม
น้ำยาซักแห้ง ผลิตภัณฑ์สำหรับ เส้นผม สารฆ่าแมลง เป็นต้น
VOCs แบ่งตามลักษณะของโมเลกุลได้เป็น 2 กลุ่มใหญ่ ๆ คือ
1. Non-chlorinated VOCs หรือ Non-halogenated hydrocarbons ได้แก่ กลุ่มไฮโดร
คาร์บอน
ระเหยที่ไม่มีธาตุคลอรีนเป็นองค์ประกอบ เช่นสารในกลุ่ม aliphatic hydrocarbons (เช่น
น้ำมันเชื้อเพลิง, ก๊าซโซลีน (gasoline) ,hexane , solvents,ในอุตสาหกรรม alcohols, aldehydes, ketone)
และกลุ่ม
aromatic hydrocarbons (เช่น toluene, benzene, ethylbenzene, xylenes, styrene, phenol)
สาร VOCs
กลุ่มนี้มาจาก การเผาไหม้กองขยะ พลาสติก วัสดุและอุปกรณ์เครื่องใช้ สีทาวัสดุเป็นต้น ซึ่งมี
ีอันตรายต่อระบบทางเดินหายใจ
2. chlorinated VOCs หรือ halogenated hydrocarbons ได้แก่ กลุ่มไฮโดรคาร์บอนระเหย
ที่มีธาตุคลอรีนเป็นองค์ประกอบ ได้แก่ สารเคมีสังเคราะห์ในอุตสาหกรรม
สาร
chlorinated VOCs นี้มีความ
เสถียรและสะสมได้นานในสิ่งแวดล้อม มากกว่ากลุ่มแรก (non-chlorinated
VOCs) เพราะมีพันธะระหว่าง
คาร์บอนและธาตุกลุ่มฮาโลเจนซึ่งทนทานและ ยากต่อการ สลายตัวในธรรมชาติ อันตรายของสารกลุ่มนี้คือ
จะรบกวนการทำงานของสารพันธุกรรม ยับยั้งปฎิกริยาชีวเคมีในเซลล์และมีฤทธิ์ในการก่อมะเร็ง

รูปที่ 2.8 ตัวอย่างของสาร VOC
สาร VOCs เข้าสู่ร่างกายได้ 3 ทางคือ การหายใจ ทางปากโดยการกิน-ดื่ม และ การสัมผัสทาง
ผิวหนัง ซึ่งความเป็นพิษต่อร่างกายจะมากน้อยขึ้นอยู่กับปัจจัยดังต่อไปนี้
1. ช่วงครึ่งชีวิตของสาร VOCs ในร่างกาย
2. สภาวะความสมบูรณ์ของร่างกาย
3. ระบบการขับถ่ายของเสีย
สาร VOCs ถูกขับผ่านทางไตโดยปัสสาวะ ทางลมหายใจ และทางตับ และน้ำดี
สาร VOC มีอันตรายต่อมนุษย์ ดังนี้คือ
ผลต่อระบบภูมิคุ้มกันทำให้ประสิทธิภาพลดลง
ผลกระทบ ผลกระทบต่อระบบประสาท เช่น มีฤทธิ์กดประสาท, ทำลายระบบประสาทส่วนกลาง
ผลกระทบต่อด้านอื่นๆ เช่น ระบบพันธุกรรม ระบบฮอร์โมน ระบบสืบพันธุ์ และระบบประสาท
อาจก่อ ให้เกิดโรคมะเร็ง
การป้องกันและการแก้ไข
การป้องกันและการแก้ไขอาจทำได้โดย ป้องกันมิให้มีการใช้สารที่อันตรายสูงต่อสุขภาพ
โดยไม่จำเป็นหรือมีมาตรการในการจัดควบคุมให้สารกลุ่มปนเปื้อน ในสิ่งแวดล้อมอยู่ในระดับที่เหมาะสมต่อ
สิ่งมีชีวิต
ฝุ่นละออง (Suspended Particulate Matter)
ฝุ่นละอองในบรรยากาศเป็นปัญหามลพิษทางอากาศที่สำคัญที่สุดของกรุงเทพมหานครและ
เมืองใหญ่ๆ ซึ่งส่งผลกระทบต่อสุขภาพอนามัยของประชาชนทั้งทางตรงและทางอ้อมประกอบด้วยสารต่างๆ
ทั้งที่เป็นของแข็ง และ ของเหลว ที่กระจายอยู่ในบรรยากาศ เป็นกลุ่มของโมเลกุลที่มองด้วยตาเปล่าไม่เห็น
มีขนาดตั้งแต่ 0.002 ไมครอนไปจนถึง ฝุ่นที่มีขนาดใหญ่กว่า 500 ไมครอน ซึ่งแบ่งเป็น 3 ประเภทดังนี้
• ฝุ่นขนาดเล็กกว่า 10 ไมครอน
• ฝุ่นรวม (Total Suspended Particulate: TSP) มีขนาดเล็กกว่า 100 ไมครอน
• ฝุ่นหนัก (dust fall) ฝุ่นขนาดตั้งแต่ 100 ไมครอนขึ้นไป
แหล่งที่มาของฝุ่นละอองในบรรยากาศ แบ่งเป็น 2 ประเภทใหญ่ๆ
1. ฝุ่นละอองตามธรรมชาติ ( natural particle ) เช่น ดิน ทราย ละอองน้ำ เขม่าควันจากควันป่า ฝุ่นเกลือ
จากทะเล
2. ฝุ่นละอองที่เกิดจากกิจกรรมที่มนุษย์ ( man-made particle )
การคมนาคมขนส่ง
การก่อสร้าง การปรับปรุงสาธารณูปโภค
โรงงานอุตสาหกรรม การเผาไหม้เชื้อเพลิง
โลหะหนักและสารประกอบของโลหะหนัก เช่น แคดเมียม (Cd) ตะกั่ว (Pb) โครเมียม(Cr) ทำให้เกิด
ฝุ่นส่วนใหญ่ โดยจะเป็นในรูปของอนุภาคและจะแตกตัวในน้ำและดินโดยไปสะสมอยู่ได้ทั้งแบบแห้งและเปียก
(dry and wet depositions)และก่อให้เกิดปัญหาน้ำและดินปนเปื้อนส่วนใหญ่แคดเมียมมาจากโรงงานถลุงสังกะสี
โรงงานผลิตรงควัตถุแคดเมียม (cadmium pigment) เป็นต้น ตะกั่วมาจากโรงงานถลุงตะกั่ว โรงงานผลิตรงควัตถุ (pigment) โรงงานแก้ว และรถยนต์ที่ใช้น้ำมันเติมสารตะกั่ว ส่วนแหล่งโครเมียม ได้แก่โรงงานผลิตรงควัตถุโครเมี่ยม
(chromium pigment) เป็นต้น
ผลเสียของฝุ่นละอองในด้านต่างๆ แบ่งได้ดังนี้คือ
1. ผลต่อสภาพบรรยากาศทั่วไป ทำให้ทัศนวิสัยไม่ดี เนื่องจากเป็นอนุภาคของแข็งที่ดูดซับ
และหักเหแสงได้ ทั้งนี้ขึ้นอยู่กับขนาดและความหนาแน่น และองค์ประกอบของฝุ่นละออง
2. ผลต่อวัตถุและสิ่งก่อสร้าง ทำให้เกิดความสกปรกแก่ อาคาร และสิ่งก่อสร้าง และทำอันตรายต่อวัตถุ
ุและสิ่งก่อสร้างได้ เช่นกัดกร่อนผิวหน้าของโลหะหินอ่อนหรือวัตถุอื่นๆ เช่น รั้วเหล็ก หลังคาสังกะสี รูปปั้น ฯลฯ
3. ผลต่อสุขภาพอนามัยของมนุษย์ ทำให้เกิดอาการระคายเคืองตาและ ยังส่งผลต่อระบบหายใจซึ่ง
ขึ้นอยู่กับขนาดของฝุ่นละออง ละอองขนาดใหญ่จะถูกดักไว้ที่ขนจมูกส่วนฝุ่นละอองที่สามารถเข้าสู่ระบบ
ทางเดินหายใจของมนุษย์ได้มีขนาดเล็กกว่า 10 ไมครอน เมื่อเข้าสู่ระบบทางเดินหายใจทำให้ระคายเคืองแสบจมูก
ไอ จาม มีเสมหะหรือมีการสะสมของฝุ่นในถุงลมปอด ทำให้การทำงานของปอดเสื่อมลง
 
|

