![]()
1.หลักการในการวิเคราะห์
อิเล็กโทรแกรวิเมทรี
จัดเป็นเทคนิคการวิเคราะห์เชิงไฟฟ้าวิธีหนึ่ง โดยมีการจัดเซลล์แบบอิเล็กโทรไลต์
กล่าวคือ จำเป็นต้องให้พลังงานไฟฟ้าจากภายนอกเข้าไปในเซลล์ โดยกระแสไฟฟ้าที่ผ่านที่เข้าไปนี้
จะต้องเป็นไฟฟ้ากระแสตรง (D.C.) เท่านั้น ศักย์ไฟฟ้าภายนอกที่ให้กับเซลล์จะต้องมีค่าเท่ากับค่าศักย์การแตกตัวของสารที่ต้องการจะวิเคราะห์
ในที่สุดก็จะทำให้เกิดการแยกสลายสารตัวอย่างด้วยไฟฟ้า ในการวิเคราะห์จำเป็นจะต้องมีการกวนสารละลายตลอดเวลา
เพื่อช่วยเร่งและพาไอออนของสารตัวอย่างไปอยู่ใกล้ ๆ กับผิวของขั้วไฟฟ้าและเกิดปฏิกิริยาบนขั้วไฟฟ้า
ผลที่ได้จากปฏิกิริยานั้นจะทำให้เกิดของแข็งของสารตัวอย่างเกาะอยู่บนขั้วไฟฟ้าที่เรียกว่า
ขั้วใช้งาน (working electrode) และเมื่อสารตัวอย่างเกิดปฏิกิริยาอย่างสมบูรณ์แล้ว
น้ำหนักของของแข็งที่เพิ่มขึ้นบนขั้วไฟฟ้า ก็จะถูกนำไปคำนวณหาปริมาณของสารตัวอย่างที่อยู่ในสารละลาย
ดังนั้นเทคนิคนี้จึงเกี่ยวข้องกับการคำนวณน้ำหนักของสารตัวอย่างจากผลต่างของน้ำหนักขั้วไฟฟ้าก่อนและหลัง
การวิเคราะห์
2.เทคนิควิธีวิเคราะห์ด้วยอิเล็กโทรแกรวิเมทรี
การวิเคราะห์เชิงไฟฟ้าด้วยเทคนิคอิเล็กโทรแกรวิเมตรีสารมารถแบ่งออกได้เป็น 2 วิธี ดังนี้
2.1 อิเล็กโทรแกรวิเมตรีแบบกระแสคงที่ หรือแบบไม่ควบคุมศักย์ขั้วไฟฟ้า
การวิเคราะห์หาปริมาณของสารตัวอย่างด้วยเทคนิคอิเล็กโทรแกรวิเมตรีวิธีนี้สามารถกระทำได้ง่าย โดยการต่อเซลล์เข้ากับแหล่งให้พลังงานไฟฟ้าจากภายนอกชนิดกระแสตรง เช่น แบตเตอรี เข้าไปในเซลล์ การวิเคราะห์ด้วยวิธีนี้ไม่จำเป็นต้องอาศัยอุปกรณ์ที่ซับซ้อนมาก ซึ่งแสดงได้ดังรูป
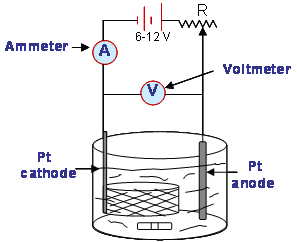
เมื่อเซลล์ได้รับพลังงานเท่ากับศักย์ไฟฟ้าการแตกตัวของสารตัวอย่าง ซึ่งจะมีอุปกรณ์ที่ควบคุมกระแสให้อยู่ในระดับหนึ่ง โดยกระแสที่ให้กับเซลล์จะต้องมากพอที่จะทำให้เกิดการไหลของกระแสเกิดขึ้นภายในเซลล์ และทำให้ปฏิกิริยาดำเนินต่อไปได้จนเสร็จสิ้นและสมบูรณ์ ปฏิกิริยาที่เกิดขึ้นภายในเซลล์จะทำให้เกิดการแยกของสารตัวอย่าง ส่งผลให้สารตัวอย่างที่ต้องการแยกจะไปพอกพูนบนขั้วไฟฟ้า
2.2
อิเล็กโทรแกรวิเมตรีแบบควบคุมศักย์ขั้วไฟฟ้า
การวิเคราะห์ด้วยวิธีนี้
ก็จะมีการให้ศักย์ไฟฟ้าชนิดกระแสตรงจากภายนอกเข้าไปในเซลล์เช่นกัน จึงจะทำให้เกิดการแยกของสารตัวอย่างในสารละลาย
แต่ศักย์ไฟฟ้าที่ให้เข้าไปจะต้องมีการควบคุมเพื่อไม่ให้สารชนิดอื่นปะปนกับสารตัวอย่างในขั้นตอนการวิเคราะห์
ซึ่งทำให้การวิเคราะห์มีความถูกต้อง อุปกรณ์ที่ทำหน้าที่ควบคุมศักย์ไฟฟ้าที่ให้กับเซลล์เรียกว่า
โพเทนชิออสแตท (potentiostat) การจัดเรียงตัวของเซลล์ สามารถแสดงได้ดังรูป
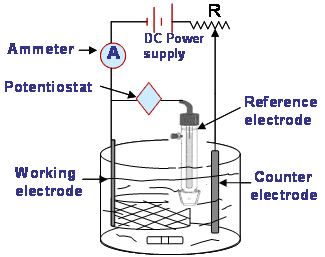
3. การประยุกต์ใช้ในการวิเคราะห์
การวิเคราะห์ด้วยเทคนิคอิเล็กโทรแกรวิเมตรีมีประโยชน์มากในการวิเคราะห์หาชนิดและปริมาณของไอออนโลหะในสารละลายตัวอย่าง
เช่น Cu2+, Cd2+, Zn2+ และ Pb2+
ถึงแม้ว่าโลหะแต่ละชนิดจะมีค่าศักย์มาตรฐานต่างกันเพียงมิลลิโวลต์ (mV) ก็สามารถวิเคราะห์ได้
โดยไม่เกิดการรบกวนของโลหะที่ไม่ต้องการ ทำให้โลหะที่ได้มีความบริสุทธิ์
ปราศจากสิ่งเจือปน