"ไฟฟ้าเคมี" เป็นความสัมพันธ์ระหว่างปฏิกิริยาเคมีและพลังงานไฟฟ้า ซึ่งกระบวนการทางไฟฟ้าเคมีจะเกิดจากการถ่ายโอนอิเล็กตรอนจากสารหนึ่งไปยังสารหนึ่ง และเมื่อมีการถ่ายโอนอิเล็กตรอน ปฏิกิริยาเคมีก็จะสามารถทำให้เกิดพลังงานไฟฟ้าได้ ในทำนองกลับกันพลังงานไฟฟ้าก็สามารถทำให้เกิดปฏิกิริยาเคมีได้เช่นกัน ปฏิกิริยาที่มีการถ่ายโอนอิเล็กตรอนนี้เรียกว่า ปฏิกิริยารีดอกซ์ (Redox Reaction)
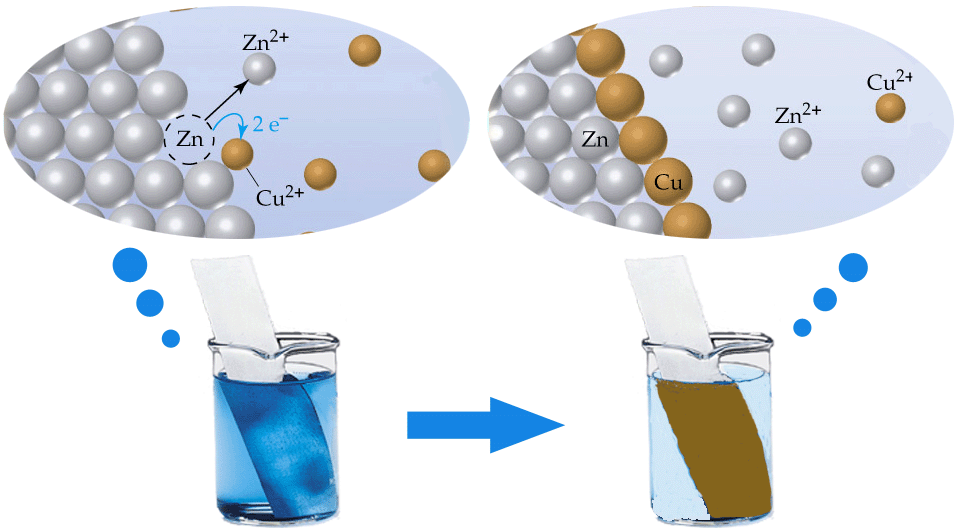
ปฏิกิริยารีดอกซ์ หรือปฏิกิริยาออกซิเดชัน-รีดักชัน (Oxidation-Reduction Reaction) จะเกิดสองปฏิกิริยาย่อยควบคู่กันไปเสมอ นั่นคือ ปฏิกิริยาออกซิเดชัน (Oxidation Reaction) และ ปฏิกิริยารีดักชัน (Reduction Reaction) ปฏิกิริยารีดอกซ์ส่วนมากจะเกิดขึ้นเองตามธรรมชาติ เช่น การนำโลหะสังกะสี (Zn) จุ่มลงไปในสารละลายของทองแดง (Cu2+) ดังรูป
ปฏิกิริยาที่เกิดขึ้นเป็นไปตามสมการ อิเล็กตรอนจะถูกถ่ายโอนจาก Zn ไปยัง Cu2+ ในสารละลายได้โดยตรง สิ่งที่จะสังเกตเห็นได้ชัดเจนก็คือ แผ่นสังกะสีจะกร่อน มีตะกอนของทองแดงเกิดขึ้นบนแผ่นสังกะสี และเมื่อตั้งทิ้งไว้สารละลายสีฟ้าของ Cu2+ จะค่อย ๆ เปลี่ยนเป็นไม่มีสี โดยเกิดปฏิกิริยาย่อย หรือที่เรียกว่าครึ่งปฏิกิริยา (half-reaction) คือ ปฏิกิริยาออกซิเดชัน
เป็นปฏิกิริยาที่มีการให้อิเล็กตรอน โดย Zn ให้อิเล็กตรอนแล้วกลายเป็น
Zn2+ ปฏิกิริยารีดักชันเป็นปฏิกิริยาที่มีการรับอิเล็กตรอน โดย Cu2+ รับอิเล็กตรอนแล้วกลายเป็นอะตอมของ Cu Cu2+(aq)
+ 2e- Cu2+ เมื่อรับอิเล็กตรอนแล้วมีเลขออกซิเดชันลดลงจาก +2 เป็น 0 ปฏิกิริยารีดักชันจึงเป็นปฏิกิริยาที่มีการลดลงของเลขออกซิเดชัน และเรียกสารที่มีเลขออกซิเดชันลดลงหรือมีการรับอิเล็กตรอน (Cu2+) ว่า ตัวออกซิไดซ์ (Oxidizing agent) เมื่อรวมปฏิกิริยา (1) และ (2) จะได้ปฏิกิริยาดังสมการ Zn(s)
+ Cu2+(aq) ปฏิกิริยา (3) เรียกว่าปฏิกิริยาออกซิเดชัน-รีดักชัน หรือปฏิกิริยารีดอกซ์นั่นเอง โดย Zn รีดิวซ์ Cu2+ ให้เป็น Cu และ Cu2+ ออกซิไดซ์ Zn ให้กลายเป็น Zn2+ หรืออาจกล่าวว่า Cu2+ ถูกรีดิวซ์โดย Zn และ Zn ถูกออกซิไดซ์โดย Cu2+ Zn จึงเป็นตัวรีดิวซ์ และ Cu2+ เป็นตัวอกซิไดซ์ ตัวอย่างปฏิกิริยารีดอกซ์เพิ่มเติม
H2(g)
+ I2(g)
2KClO3(s)
2Na(s)
+ H2O(l)
Cu(s)
+ 2AgNO3(aq)
Cl2(g)
+ 2Br-(aq) บอกได้หรือไม่ว่าแต่ละปฏิกิริยามีสารตัวใดเป็นตัวรีดิวซ์ และสารตัวใดเป็นตัวออกซิไดซ์ ***การรวมปฏิกิริยาต้องตรวจสอบจำนวนอิเล็กตรอนที่ให้และที่รับของทั้งสองครึ่งปฏิกิริยาให้เท่ากันก่อน
LAnOx vs GRedCat LAnOx: Lose electrons/mass: Anode: Oxidized(Oxidation) GRedCat: Gain electrons/mass: Reduced(Reduction): Cathode
|
||||||||||||