![]()

จ๊าค อเล็กซองดร์ เซซา ชาร์ล (Jacques Alexandre César Charles, ค.ศ.1746 - 1823)
เราทราบมาแล้วว่าสสารที่อยู่ในสถานะแก๊สมีความหนาแน่นน้อย เมื่อพิจารณาระยะห่างระหว่างโมเลกุลของแก๊สจะมีระยะทางมากกว่าของแข็งและของเหลว ตามลำดับ เมื่อได้รับความร้อนเพิ่มขึ้น แก๊สจะขยายตัวมากกว่าการขยายตัวของของเหลวและของแข็ง ตามลำดับ
![]()
ทำไม ข้างกระป๋องสเปรย์สี หรือน้ำหอมต่างๆ จึงมีคำเตือนข้อหนึ่งที่บอกว่า ห้ามนำกระป๋องสเปรย์ไปเผาไฟ หรือนำไปใกล้ความร้อน
สำหรับการทดลองเกี่ยวกับแก๊สของนักวิทยาศาสตร์ชาวฝรั่งเศส จ๊าค ชาร์ล สนใจศึกษาสมบัติของแก๊สเช่นเดียวกัน โดยการทดลองของชาร์ล ได้ศึกษาความสัมพันธ์ของปริมาตรแก๊สเมื่ออุณหภูมิเปลี่ยนแปลงไป ชาร์ลได้สนใจศึกษาเรื่องแก๊สเนื่องจากในสมัยนั้นมี การใช้อากาศร้อนทำให้บอลลูนลอยบนอากาศกำลังเป็นเรื่องที่นิยมและน่าสนใจอย่างมาก เป็นเรื่องที่นักวิทยาศาสตร์ต่างสนใจที่จะทำให้บอลลูนลอยขึ้นไปได้สูงๆ และลอยได้นานขึ้นจึงมีการพัฒนาเพื่อเพิ่มประสิทธิภาพของบอลลูนของนักวิทยาศาสตร์ต่างๆ ความสัมพันธ์ระหว่างการขยายตัวของแก๊สกับอุณหภูมิจึงเป็นเรื่องที่น่าสนใจ
รวมทั้งชาร์ลก็เช่นเดียวกัน ในการทดลองของเขา เขาได้ใช้เครื่องมือเป็นหลอดแก้วรูปตัวเจ(J form) คล้ายๆ กับของ โรเบิร์ต บอยล์ ภายในหลอดบรรจุแก๊สปริมาณหนึ่งเอาไว้ เมื่อเขาให้ความร้อนแก่แก๊สที่อยู่ในหลอด เขาพบว่าแก๊สได้ขยายตัวมีปริมาตรเพิ่มขึ้น
รูปแสดงความสัมพันธ์ของปริมาตรและอุณหภูมิ ที่ความดันคงที่
จากรูปเป็นท่อทรงกระบอกบรรจุแก๊สปริมาณคงที่ค่าหนึ่ง และที่ความดันคงที่เท่ากับ 1 บรรยากาศ ในรูปแก๊สปริมาตร 0.5 ลิตร ที่อุณหภูมิ 300 K เมื่อให้ความร้อนกับแก๊สเหล่านี้ จนมีอุณภูมิเป็น 600 K แก๊สจะขยายตัวมีปริมาตร เท่ากับ 1 ลิตรตามรูป และทำนองเดียวกันถ้าลดอุณหภูมิจาก 600 K ลงมาที่ 300 K เท่าเดิมแก๊สก็จะหดตัวมีปริมาตร 0.5 ลิตรเช่นเดิม
จากการทดลองของชาร์ล พบว่าปริมาตรของแก๊สจะเพิ่มขึ้น ตามอุณหภูมิที่เพิ่มขึ้น และในทางตรงกันข้ามถ้าลดอุณหภูมิลงปริมาตรของแก๊สก็จะลดลงด้วย มีลักษณะเช่นเดียวกับรูปด้านบน
โดยเขาพบว่า ถ้าตอนเริ่มต้นทดลอง อุณหภูมิของแก๊ส อยู่ที่ 0 องศาเซลเซียส และปริมาตรแก๊สเริ่มต้นที่ค่าหนึ่ง
-
ถ้าให้อุณหภูมิเพิ่มขึ้นไปเป็น 1 องศาเซลเซียส ปริมาตรของแก๊สจะเพิ่มขึ้นจากเดิมประมาณ![]() เท่า
เท่า
-
ถ้าอุณหภูมิเพิ่มขึ้นไปเป็น 2 องศาเซลเซียส ปริมาตรแก๊สจะเพิ่มจากเดิมประมาณ
![]() เท่าและ
เท่าและ
-
ถ้าอุณหภูมิเพิ่มไปเป็น 10 องศาเซลเซียส ปริมาตรแก๊สเพิ่มจากเดิมอีกประมาณ
![]()
สัดส่วนนี้จะเป็นไปตามอุณหภูมิที่เพิ่มขึ้นนั้น
ปริมาตรจะแปรผันตรงตามอุณหภูมิ เรากำหนดให้ค่าสัดส่วน ![]() เป็นค่าคงที่ค่าหนึ่งใช้สัญลักษณ์เป็น
แอลฟา(
เป็นค่าคงที่ค่าหนึ่งใช้สัญลักษณ์เป็น
แอลฟา(![]() ) โดยค่า
) โดยค่า
![]() ซึ่งเศษส่วนนี้ในความรู้สึกของเราก็ถือว่าน้อยมาก แต่ถ้าอุณหภูมิเปลี่ยนมากๆ
ค่าเศษส่วนนี้ก็จะมีค่ามากขึ้น เช่น จาก 0 องศาเซลเซียส เพิ่มอุณหภูมิให้แก๊สขึ้นไปเป็น
100 องศา ปริมาตรแก๊สก็จะเปลี่ยนไปจากเดิมประมาณ
ซึ่งเศษส่วนนี้ในความรู้สึกของเราก็ถือว่าน้อยมาก แต่ถ้าอุณหภูมิเปลี่ยนมากๆ
ค่าเศษส่วนนี้ก็จะมีค่ามากขึ้น เช่น จาก 0 องศาเซลเซียส เพิ่มอุณหภูมิให้แก๊สขึ้นไปเป็น
100 องศา ปริมาตรแก๊สก็จะเปลี่ยนไปจากเดิมประมาณ ![]() ของหน่วยปริมาตร หรืออีกกรณีหนึ่ง ถ้าแก๊สมีปริมาณเยอะมาก ปริมาตรเริ่มต้นของแก๊สมีขนาดใหญ่
ก็จะทำให้เกิดการเปลี่ยนแปลงที่เราสังเกตได้ชัดเจนขึ้น กำหนดให้สัดส่วนเป็นค่าแอลฟา
(
ของหน่วยปริมาตร หรืออีกกรณีหนึ่ง ถ้าแก๊สมีปริมาณเยอะมาก ปริมาตรเริ่มต้นของแก๊สมีขนาดใหญ่
ก็จะทำให้เกิดการเปลี่ยนแปลงที่เราสังเกตได้ชัดเจนขึ้น กำหนดให้สัดส่วนเป็นค่าแอลฟา
(![]() )
และเมื่อนำข้อมูลการทดลองของชาร์ลไปเขียนกราฟความสัมพันธ์ระหว่างปริมาตรและอุณหภูมิในหน่วยองศาเซลเซียสจะได้กราฟดังรูป
)
และเมื่อนำข้อมูลการทดลองของชาร์ลไปเขียนกราฟความสัมพันธ์ระหว่างปริมาตรและอุณหภูมิในหน่วยองศาเซลเซียสจะได้กราฟดังรูป
เราจะได้กราฟเส้นตรง จุดตัดแกน y คือปริมาตรของแก๊สที่ อุณหภูมิ 0 องศาเซลเซียส ให้เท่ากับ V0 มิลลิลิตรและเมื่อลากเส้นประไปจนปริมาตรของแก๊สเท่ากับ 0 มิลลิลิตรพบว่าเส้นกราฟตัดแกนอุณหภูมิที่ประมาณ -273 องศาเซลเซียส
จากกราฟเส้นตรงที่ได้จากการทดลองเขียนเป็นความสัมพันธ์ทางคณิตศาสตร์ระหว่างปริมาตรและอุณหภูมิได้ดังนี้
![]()
เมื่อ V = ปริมาตรของแก๊สที่สังเกต ณ อุณหภูมิใดๆ
V0 = ปริมาตรแก๊สที่ 0 องศาเซลเซียส
t = อุณหภูมิในหน่วยองศาเซลเซียส
คูณ
![]() เข้าไปจะได้
เข้าไปจะได้
![]() ....................................................1
....................................................1
เมื่อแทนค่า
![]() ในสมการ
1 จะได้
ในสมการ
1 จะได้
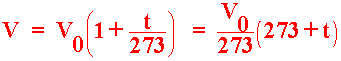 ........................................(2)
........................................(2)
และกำหนดให้
![]() สมการ (2) จะกลายเป็น
สมการ (2) จะกลายเป็น
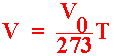 ....................................................................(3)
....................................................................(3)
หรือ
![]() ...................................................(4)
...................................................(4)
เมื่อ k เป็นค่าคงที่
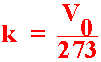
และ T ก็จะเป็นอุณหภูมิทำให้ปริมาตรของแก๊สแปรผันตรงแบบเป็นเส้นตรง
จากสมการ (3) จะพบว่าถ้า แก๊สมีปริมาตร(V) เท่ากับ 0 พจน์ T จะต้องเป็น 0 ด้วย (เพราะ k เป็นค่าคงที่มากกว่า 1 ) นั่นแสดงว่าอุณหภูมิในหน่วยองศาเซลเซียสที่ทำให้แก๊สมีปริมาตรเป็น 0 จริงๆ จะเท่ากับ
T = 273 + t
เมื่อ T = 0 ; 0 = 273+t
นั่นหมายความว่า t = -273 องศาเซลเซียส
ที่อุณหภูมิ -273 องศาเซลเซียสแก๊สจะมีปริมาตรเป็น 0 ซึ่งอุณหภูมินี้เป็นอุณหภูมิ 0 ที่แท้จริง ดังนั้นจึงกำหนดให้ที่อุณหภูมินี้เป็นหน่วยอุณหภูมิที่เริ่มจาก 0 จริงๆ และหน่วยอุณหภูมิใหม่ นี้คือ เคลวิน (K)นั่นเอง
![]()
แก๊สไนโตรเจนปริมาตร 1.5 ลิตร อุณหภูมิ 25 oC เมื่อให้ความร้อนกับแก๊สจนอุณหภูมิเท่ากับ 350 oC ปริมาตของแก๊สไนโตรเจนจะเป็นเท่าใดเมื่อความดันแก๊สไม่เปลี่ยนแปลง