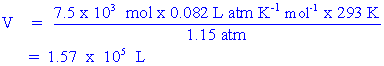![]()
จากการทดลองและข้อสรุปของนักวิทยาศาสตร์หลายๆ คนที่ศึกษาเรื่องแก๊สเราจะเห็นว่า สมบัติของแก๊สมีความสัมพันธ์กันด้วยตัวแปรคล้ายๆ กัน คือ ทุกคนต่างก็ดูที่ปริมาตรของแก๊สที่เปลี่ยนไป ด้วยการกำหนดตัวแปรต้นแตกต่างกันออกไป
บอยล์ เมื่อเปลี่ยนความดันของแก๊ส ปริมาตรจะเป็นอย่างไร
ชาร์ล เมื่อเปลี่ยนอุณหภูมิของแก๊ส ปริมาตรจะเป็นอย่างไร
อาโวกาโดร เมื่อเปลี่ยนจำนวนโมลหรือจำนวนโมเลกุลของแก๊ส ปริมาตรจะเป็นอย่างไร
และทุกคนก็ได้ข้อสรุปดังที่ได้นำเสนอกฏของทุกคนมาแล้ว ถ้าเรารวบรวมกฎที่เกี่ยวกับแก๊สที่กล่าวมาแล้วทั้งหมด เราจะได้ความสัมพันธ์ดังนี้
จาก
กฏของบอยล์ ![]()
กฎของชาร์ล
![]()
กฏของอาโวกาโดร
![]()
เราสามารถรวมกฎทั้งสามนี้เข้าเป็นสมการรวมเพียงสมการเดียวได้ดังนี้
![]()
![]()
เมื่อ
| P = ความดัน |
| V = ปริมาตร |
| n = จำนวนโมล |
| T = อุณหภูมิ(เคลวิน,K) |
สมการนี้เรียกว่า สมการแก๊สในอุดมคติ
R = ค่าคงที่ของแก๊ส (gas constant)
จากตัวแปรทั้ง 4 ตัว คือ ความดัน(P), ปริมาตร(V), จำนวนโมล(n) และอุณหภูมิ(T) เราสามารถหาค่า R ได้จากการแทนค่าตัวแปรทั้งสี่ในสมการแก๊สอุดมคติ
แก๊สอุดมคติ 1 โมล ที่สภาวะมาตรฐาน ความดันเท่ากับ 1 บรรยากาศ อุณหภูมิ 273 K มีปริมาตร 22.4 ลิตร เราจะสามารถคำนวณหาค่าคงที่ของแก๊สได้ดังนี้
จาก ![]()
![]()
นอกจากนี้ค่าคงที่ R ยังมีได้อีกในหลายหน่วย ดังนี้
![]()
![]()
แก๊สใดๆ ก็ตามที่มีพฤติกรรมเป็นไปตามกฏนี้ จะเรียกแก๊สนั้นว่าแก๊สที่มีพฤติกรรมในอุดมคติ หรือแก๊สอุดมคติ หรือแก๊สสมบูรณ์แบบ (ideal gas)
ตัวอย่างการใช้กฎของแก๊สอุดมคติ ในการคำนวณ
ตัวอย่าง 1 น้ำจำนวน 1 กรัม ระเหยกลายเป็นไอในภาชนะขนาด 10 ลิตร ความดันของน้ำจะเป็นเท่าใดเมื่อการระเหยเป็นไอสมบูรณ์ที่อุณหภูมิ 200 องศาเซลเซียส
วิธีคำนวณ
จาก
![]()
เราต้องการหาความดันของไอน้ำ
จำนวนโมล (n) ของน้ำ
![]()
และอุณหภูมิสัมบูรณ์ เท่ากับ
![]()
แทนค่า V = 10 L , T = 473 K และ n = 0.056 mol
ความดันจะเท่ากับ
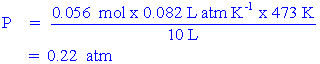
ตัวอย่าง 2 บอลลูนลูกหนึ่งบรรจุแก๊สฮีเลียม (He) หนัก 30 กิโลกรัม บอลลูนลูกนี้จะมีปริมาตรเท่าใด ถ้าความดันของแก๊สฮีเลียมเป็น 1.15 atm ณ อุณหภูมิ 20 องศาเซลเซียส
วิธีทำ
จาก
![]()
เราอยากทราบปริมาตรของบอลลูน
ก่อนอื่นต้องคำนวณหา จำนวนโมลของแก๊สฮีเลียม หนัก 30 กิโลกรัม ก่อน
เราทราบมาแล้วว่า ฮีเลียมจำนวน 1 โมล มีน้ำหนัก 4 กรัม หรือ 0.0040 kg
![]()
อุณหภูมิต้องเปลี่ยนเป็นหน่วยเคลวินก่อน
![]()
ดังนั้น ปริมาตรสามารถคำนวณได้ดังนี้