เอนไซม์ (enzyme) คือ สารที่ทำหน้าที่เร่งปฏิกิริยาต่างๆในสิ่งมีชีวิต (biocatalyst) ทำให้อัตราเร็วของปฏิกิริยานั้นๆ เพิ่มสูงขึ้นได้ถึง หนึ่งล้านถึงล้านล้านเท่า (106-1012 ) ของปฏิกิริยาเดิมที่ไม่มีเอนไซม์เป็นตัวเร่ง หรือพูดอีกแบบหนึ่งว่า เอนไซม์ทำให้เกิดปฏิกิริยาได้รวดเร็วขึ้น สารที่เข้าทำปฏิกิริยาหรือสารตั้งต้นในปฏิกิริยา เรียกว่า ซับสเตรต (substrate) จะเข้าจับหรือทำปฏิกิริยากับเอนไซม์ แล้วได้ผลิตภัณฑ์ (product) ออกมา
การเร่งปฏิกิริยา (catalysis) หมายถึง การที่สารที่เรียกว่าตัวเร่งปฏิกิริยาหรือคะตะลิสต์ (catalyst) สามารถเปลี่ยนแปลงอัตราเร็วของปฏิกิริยาเคมีให้เร็วขึ้นได้ ในปี พ.ศ. 2437 ออสท์วอลด์ (Ostwald) ให้คำจำกัดความของ ตัวเร่งปฏิกิริยาว่าเป็น "สารที่ทำให้อัตราเร็วของปฏิกิริยาเพิ่มขึ้น และเมื่อปฏิกิริยาสิ้นสุดแล้ว ตัวเร่งปฏิกิริยาจะไม่มีการเปลี่ยนแปลงใดๆ ทำให้สามารถเร่งปฏิกิริยาได้ซ้ำแล้วซ้ำอีก"
เอนไซม์มีลักษณะพิเศษแตกต่างจากคะตะลิสต์ (catalyst) ในปฏิกิริยาเคมีธรรมดา ดังต่อไปนี้
1. เอนไซม์เป็นคะตะลิสต์ที่มีความจำเพาะ (specificity) ทั้งต่อ ซับสเตรต ผลิตภัณฑ์ และปฏิกิริยาที่เร่ง (reaction) นั่นคือ เอนไซม์ชนิดหนึ่งๆ จะสามารถเร่งปฏิกิริยาเคมีที่มีซับสเตรตชนิดใดชนิดหนึ่งแล้วได้ผลิตภัณฑ์โดยเฉพาะ แต่อย่างไรก็ตามการเร่งปฏิกิริยา ก็มีความยืดหยุ่น (flexibility) ไม่ได้เป็นเอนไซม์หนึ่งชนิดต่อซับสเตรตหนึ่งชนิด เสมอไป เพราะเอนไซม์บางชนิดจะมีความจำเพาะมาก หรือ น้อยแตกต่างกันออกไปซึ่งความจำเพาะนี้จะอธิบายในบทต่อไป (บทที่ 4 เอนไซม์มีความจำเพาะ)
2. เอนไซม์ปริมาณน้อย ๆ ก็สามารถเร่งปฏิกิริยาได้อย่างมีประสิทธิภาพ (effciency)
คือ ความเข้มข้นของเอนไซม์ที่ใช้ในปฏิกิริยาจะน้อยมาก (หน่วย ไมโครโมลาร์
: ![]() ) เมื่อเทียบกับความเข้มข้นของซับสเตรต
(หน่วย มิลลิโมลาร์ :
) เมื่อเทียบกับความเข้มข้นของซับสเตรต
(หน่วย มิลลิโมลาร์ : ![]() )
)
3. เอนไซม์จะไม่มีการเปลี่ยนแปลงใดๆหลังจากที่เกิดการเร่งปฏิกิริยาแล้ว ทำให้เกิดปฏิกิริยาได้ใหม่ โดยสามารถบอกได้เป็นค่าที่เรียกว่า turnover number คือ ค่าที่บอกว่าเอนไซม์หนึ่งโมเลกุลสามารถเร่งปฏิกิริยาเปลี่ยนซับสเตรต เพื่อให้ได้ผลิตภัณฑ์ ได้จำนวนกี่ครั้งในหนึ่งหน่วยเวลา
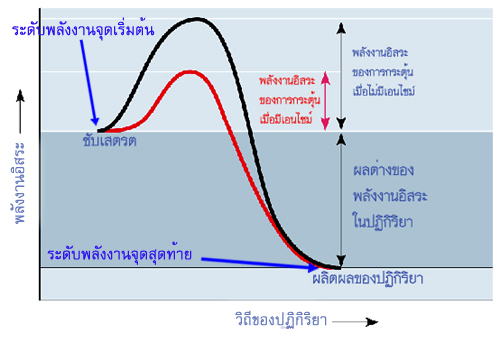
4. เอนไซม์จะไม่เปลี่ยนแปลงค่าของผลต่างของพลังงานอิสระ(free energy change, G)หรือค่าคงที่สมดุลของปฏิกิริยา (equilibrum constant)ของปฏิกิริยา คือ ไม่เปลี่ยนแปลงระดับพลังงานที่จุดเริ่มต้นและจุดสุดท้ายในปฏิกิริยา เพียงแต่ไปเร่งอัตราเร็วให้ไปสู่สมดุลได้เร็วขึ้น โดยลดพลังงานกระตุ้น (activation energy) หรือพลังงานอิสระของการกระตุ้น (free energy of activation)ลง (บทที่ 4 เอนไซม์เป็นตัวเร่งปฏิกิริยาในเซลล์)
5. เอนไซม์สามารถเร่งปฏิกิริยาได้โดยไม่ต้องอาศัยความอุณหภูมิและความดันที่สูง
เพราะตัวเร่งปฏิกิริยาทางเคมี จะต้องใช้อุณหภูมิ ความดันสูงๆ หรืออาจจะต้องใช้กรดหรือเบสแก่
จึงจะเร่งปฏิกิริยาได้
ตัวอย่างเช่น
ในการย่อยสลายพันธะเปปไทด์ในสายโพลีเปปไทด์ เช่น เนื้อสัตว์ จะต้องใช้กรดแก่
(6 M HCl) ที่ 120oC เป็นเวลา 10-24 ชั่วโมง แต่ถ้าใช้เอนไซม์ที่ย่อยโปรตีน
เช่น ไคโมทริปซิน ก็จะใช้เวลาน้อยกว่า ที่ pH 7-8 และอุณหภูมิประมาณ 37oC
ได้

